
Universitätsinstitut für Medizinisch-Chemische Labordiagnostik - Zentrallabor LKH
Landeskrankenhaus
Müllner Hauptstraße 48
A-5020 Salzburg
Fax: +43 (0) 5 7255 – 23198
Email: zentrallabor-office@salk.at
Prim. Univ.-Prof. Dr Elisabeth Haschke-Becher
Fax: +43 (0) 5 7255 – 23198
Email: e.haschke-becher@salk.at
Umstellung der INR-Messung
(22.08.2013)
Mit heutigem Datum erfolgt die Umstellung der INR Berechnung auf internationale Standards. Künftig basiert die Berechnung der INR-Werte im UIMCL (Zentrallabor) nicht wie bisher auf dem Ergebnis des "Thrombotests", sondern auf dem Ergebnis der Messung der "Prothrombinzeit" (PZ, PTZ, Quick, etc.).
Vergleiche ergaben dadurch um ca. 11% niedrigere Ergebnisse wie bisher.
Durch die Umstellung wird eine Verbesserung der Vergleichbarkeit der INR-Ergebnisse zwischen den Labors und eine Standardisierung nach WHO Richtlinine erzielt.
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Monitoring der neuen Antikoagulanzien (NOACs)
(12.11.2012)
Das Zentrallabor bietet ab sofort folgende neue Analysen an:
Andere alternative Gerinnungskemmer wie Arixtra® oder Orgaran® können bereits seit längerer Zeit bei uns monitiert werden.
Detaillierte Informationen zu den einzelnen Wirkstoffen und deren Messung finden Sie in unserer Analyse-Datenbank.
Anzoforder sind die Analysen am A-Schein des Zentrallabors bzw. am Routine-Schein der CDK.
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Methodenumstellung von Willebrand Aktivität
(29.09.2011)
Anstatt der "Ristocetin-CoFaktor-Aktivität" wird ab nun die "von Willebrand Aktivität" (vW-Ac) bestimmt. Das Testprinzip dieser Methode variiert leicht, die Aussage ist jedoch dieselbe. Auch die vW-Ac wird für die Beurteilung der Funktionalität des vorliegenden von Willebrand Antigens (vW-Ag) herangezogen. Kombiniert man die Messungen vW-Ag und vW-Ac so kann man grob zwischen den von Willebrand Syndrom Typen 1, 2 und 3 differenzieren.
Die neue Methode ist wesentlich stabilier und weniger von Produktionsengpässen seitens der Zulieferfirmen abhängig, sodas wir mit dieser neuen Methode eine durchgehende Analytik mit gleichbleibend hoher Qualität anbieten können.
Vergleichsmessungen zwischen der Ristocetin-CoFaktor-Aktivität und der vW-Ac ergaben eine ausgezeichnete Korrelation (r2 = 0,964) - s. Grafik.
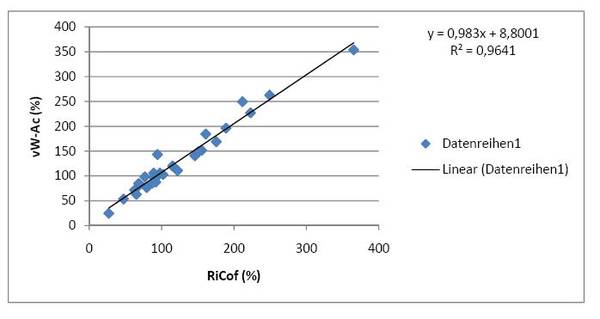
Anforderung: Weiterhin am G-Schein
Material: Weiterhin Citrat-Plasma
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Fibrinogen Antigen (immunologisch)
(3.09.2010)
Aufgrund des vermehrten Aufkommens neuer Gerinnungshemmer, haben wir die Bestimmung des Fibrinogen-Antigens in unser Analysenspektrum aufgenommen.
Die Aktivitätsbestimmung des Fibrinogen nach Clauss (derzeit die Standardmethode zur Bestimmung von Fibrinogen) kann von diesen neuen Antikoagulantien, v.a. von den direkten Thrombininhibitoren, beeinflusst werden. So kann die Fibrinogen-Aktivitätsbestimmung fälschlicherweise zu niedrig ausfallen.
Einen Überblick über die Auswirkungen von einigen der neuen Gerinnungshemmer auf die Fibrinogen-Aktivitätsmessung nach Clauss gibt folgende Tabelle:
|
Antikoagulans |
|
|
|
|
Wirkstoff |
Handelsname |
Hemmt |
Fibrinogen Aktivität |
|
Agatroban |
Argatra® |
lla (direkt) |
↓ |
|
Lepirudin |
Refludan® |
lla (direkt) |
↓ |
|
Fondaparinux |
Arixtra® |
Xa (indirekt) |
↔ |
|
Dabigatran |
Pradaxa® |
lla (direkt) |
noch keine Daten |
|
Rivaroxaban |
Xarelto® |
Xa (direkt) |
noch keine Daten |
Die Messung des Fibrinogen Antigens, kann in diesen Fällen Klarheit schaffen.
Eine weitere Indikation für die Bestimmung ist die angeborene, oder erworbene Dysfibrinogenämie, wie sie bei ausgeprägten Leberschäden, Fibrinolysetherapie, der Verbrauchskoagulapathie (DIC), Dilutionskoagulopathien, Hyperfibrinolysen, oder Fibrinogenhemmkörpern vorkommen kann.
Bestimmungsmethode: Nephelometrie
Benötigtes Material: Citrat-Plasma
Anzufordern am: G-Schein
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Umstellung der Analysenmethodik zum Nachweis von Anti-Heparin/PF4-Antikörpern (HIT II)
(24.2.2010)
Mit 24.2.2010 stellen wir die Methodik zum Nachweis von Anti-Heparin/PF4-Antikörpern um, welche ursächlich sind für das Krankheitsbild der Heparin induzierten Thrombozytopenie Typ 2 (HIT II). Ab nun wird ein Test der Fa. DiaMed als Screeninganalyse eingesetzt. Sollte dieser Test positiv ausfallen, bestätigen wird das Ergebnis mittels eines ELISA-Tests.
Durch die Einführung dieses Test ist es uns nun möglich die HIT II-Analyse kontinuierlich im Routinebetrieb anzubieten. Des Weiteren verkürzt dieser Test die Zeit bis zum Vorliegen eines Ergebnisses.
Anforderung findet sich, wie bisher, auf dem G-Schein.
ACHTUNG: Als Material für diese Analyse benötigen wir nun Serum, statt, wie bisher, Citratplasma.
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Arixtra (Fondaparinux)-Monitoring verfügbar
(18.02.2010)
Ab sofort ist es möglich in unserem Labor den Arixtra-Wirkspiegel indirekt mittels eines adaptierten Anti-Xa Tests, welcher mit Forndaparinux standardisiert wird, bestimmen zu lassen.
Anwendungsgebiete für Arixtra (Fondaparinux) sind u.A.:
Je nach Indikation sind Dosierung sowie anzustrebender Wirkspiegel (in µg/ml) unterschiedlich.
Dosierungshinweise siehe Produktinformation.
Vorläufige Richtwerte:
in Anlehnung an "Dämgen-von Brevern G et. al., Überwachung der Antikoagulanzientherapie mit Fondaparinux, Hämostaseologie 2005; 25:281-5"
Die Abnahme muss 3h Stunden nach s.c.-Applikation erfolgen, bei i.v.-Gabe im Steady state. Dieser ist nach 5 HWZ erreicht (HWZ Arixtra: 17 Stunden)
Die Analyse ist im Routinebetrieb verfügbar und online über den A-Schein anforderbar.
Für die Analyse wird Citratblut benötigt.
Für weitere Informationen lesen Sie bitte den entsprechenden Eintrag in unserer Analysen-Datenbank.
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Aktualisierung der Referenzwerte für das Heparin-Monitoring
(15.2.2010)
Mit 15.12.2010 werden die Referenzwerte für den Anti-Xa-Test (Heparin-Monitoring) den aktuellen Empfehlungen angepasst.
Die neuen Referenzwerte sind somit:
Es gilt weiterhin, dass Analysewerte nur valide sind bei Blutabnahme im Steady State. Bei s.c. Heparin-Gabe Abnahme wäre dies 4 Stunden nach Heparingabe, bei i.v. Dauerinfusion ist der Steady State nach 5 Plasmahalbwertszeiten erreicht. Die Plasmahalbwertszeit ist dosisabhängig und variiert zB bei dem UFH "HEPARIN Immuno" zwischen 1 Stunde (100 IE/kg) und 2,5 Stunden (400 IE/kg).
Wann sollte monitiert werden ?
Grundsätzlich ist ein Monitoring nicht notwendig, ausser es handelt sich um eine therapeutische Heparinisierung bei einer der folgenden Zustände:
Wenn für das Monitoring von UFH die 1.5 - 2.5fache Verlängerung der aPTT verwendet wird ist in jedem Fall auf die unterschiedliche Empfindlichkeit der verschiedenen PTT-Reagenzien auf Heparin zu achten.
Die Empfehlungen für die korrekte Einstellung der Heparine variieren leicht je nach Quelle. Zur Übersicht hier einige Auszüge:
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
ROTEM-Analysen im Zentrallabor
(21.12.2009)
Ab sofort sind bei uns im Labor nun auch sog. ROTEM-Analysen durchführbar. Die Abkürzung steht hierbei für Rotationsthrombelastometrie.
Im Gegensatz zu den klassischen Gerinnungsparametern ermöglicht die Thrombelastographie/-metrie eine Beurteilung der Gerinnselfestigkeit und -stabilität.
Indikationen für eine ROTEM Analyse
ACHTUNG: Durch die ROTEM-Analyse werden N I C H T erfasst:
Informationen zu Prinzip und Befundung finden sie auf https://www.rotem.de/ oder in der entsprechenden Fachliteratur (Zu empfehlen ist hier folgende Überblicksarbeit von Thomas Lang: J Lab Med 2007;31(6):254–261 Diagnostische Möglichkeiten und Grenzen der Thrombelastographie/-metrie - LINK)
Untersuchungsmaterial: Citratblut (grüne Sarstedt Monovette) - NICHT ZENTRIFUGIEREN !
Anforderung der Analyse:
Laufzeit:
Die Standard-Laufzeit beträgt 30 Minuten. Sollten sie eine längere Laufzeit wünschen (zB bei V.a. Hyperfibrinolyse) dann teilen sie dies bitte bei der Anforderung mit.
Präanalytik:
Proben müssen innerhalb von max 4 Stunden nach Abnahme gemessen werden.
Proben können problemlos per Rohrpost verschickt werden (wurde für unsere Hauspost eigens ausgetestet)
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
VASP-Test - Plättchenreaktivitätsindex
(15.6.2009)
Clopidogrel (zB Plavix) hat sich als potentes Medikament bei zahlreichen Indikationen erwiesen. Ein beträchtlicher Anteil der Patienten zeigt allerdings kein adäquates Ansprechverhalten auf dieses Medikament. Ein entsprechendes Monitoring konnte bei uns bisher lediglich mit der Vollblutaggregometrie durchgeführt werden. Da es hier jedoch immer wieder grenzwertige Fälle, sowie Diskordanz zwischen Labor und Klinik gegeben hat, haben wir nun einen Test aufgesetzt, welcher den Effekt von Clopidogrel auf die Thrombozyten noch sensitiver nachweisen kann.
Zusätzlich ist auch die Quantifizierung der Wirkung von Ticlopidin (zB Tiklid) auf Thrombozyten mit diesem Test möglich.
Prinzip der Methode:
Das in den Thrombozyten befindliche VASP-Protein (Vasodilator Stimulated Phosphoprotein) ist im Basalzustand nicht phosphoryliert. Die Phosphorylierung von VASP wird über den cAMP (zyklisches Adenosinmonophosphat) Weg geregelt. Während PGE1 (Prostaglandin E1) diesen Weg aktiviert (1), wird er durch ADP (Adenosindiphosphat), das auf die P2Y12-Rezeptoren (2) wirkt, gehemmt.
Misst man nun den phosphorylierten Anteil von VASP in zwei Proben, wobei jeweils eine mit PGE1 und eine weitere mit PGE1 und ADP inkubiert wurde, kann man einen sogenannten Plättchenreaktivitätsindex errechnen, mit welchem man auf die Colpidogrelwirkung zurückschließen kann.
Ein Plättchenreaktivitäsindex <50% spricht für ein gutes Ansprechen auf Clopidogrel, bzw. Ticlopidin
Benötigtes Material: Citrat-Vollblut (Bitte rufen sie uns kurz an bevor sie uns eine entsprechende Probe schicken.)
Anforderungsschein: G-Schein
Analysehäufigkeit: Mo-Fr zu den Routinelaborzeiten
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
ADAMTS-13
(15.6.2009)
ADAMTS-13 (a disintegrin-like and metalloproteinase with thrombospondin type 1 motif 13) ist ein Enzym (vWF cleaving Protease or vWF-CP), das für die physiologische Spaltung von großen von Willebrand Faktor (vWF) Molekülen verantwortlich ist. Diese großen vWF Moleküle können unter Einfluss hoher Scherkräfte zur Bildung von Plättchenthromben führen. Bei angeborener, oder erworbener Verminderung der ADAMTS-13 Aktivität können die großen vWF Multimere akkumulieren und zu Thrombosen aufgrund von Plättchenaggregation führen, was wiederum eine TTP (thrombotic thrombocytopenic purpura) zur Folge haben kann. Dieses Syndrom ist gekennzeichnet durch mikroangiopathische hämolytische Anämie und Thrombozytopenie und kann von neurologischen Symptomen, Nierenversagen, oder Fieber begleitet werden. Unbehandelt liegt die Mortalität dieser Erkrankung bei >90%.
Ab sofort kann bei uns die ADAMTS-13 Aktivität mittels eines ELISA-Tests bestimmt werden.
Aufgrund der Logistik ist dies leider nur zu den Routine-Laborzeiten möglich.
Referenzbereich: 40-130%
Benötigtes Material: Citrat-Plasma (Bitte schicken sie uns eine kurze Darstellung der Symptomatiken des Patienten mit. )
Anforderungsschein: G-Schein
Analysehäufigkeit: Mo-Fr zu den Routinelaborzeiten
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Neue Methode zur Bestimmung der Antiphospholipid-Antikörper
(18.5.2009)
Mit 18.5.2009 haben wir im Zentrallabor die Bestimmung einiger Antikörper, welche zum Nachweis eines Antiphospholipid-Syndroms wesentlich sind, umgestellt.
Für Informationen zum Antiphospholipid-Screening, siehe entsprechender Eintrag (Neuerungen/Aktuelles > Gerinnung).
Die wichtigsten Antikörper dieser Gruppe sind:
Weitere Antiphospholipid-Antikörper, die in einem weiteren Test erfasst werden können, sind:
Durch diese Umstellung auf ein automatisiertes System ist es nun möglich täglich mindestens 14 Patienten diesbezüglich abzuklären, statt wie bisher die Analyse nur einmal wöchentlich anbieten zu können.
Wir hoffen auf diese Weise zu einer besseren Versorgung der Patienten durch eine raschere Diagnosefindung beitragen zu können.
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Neue Analyse: Kaolin Clotting Time (KCT) und Rosner Index
(4.5.2009)
Zur Ergänzung des Antiphospholipid-Screenings haben wir nun die Kaolin Clotting Time (KCT) mitsamt dem Rosner Index eingeführt.
Für Informationen zum Antiphospholipid-Screening, siehe entsprechender Eintrag (Neuerungen/Aktuelles > Gerinnung).
Die KCT wird angewandt zur Detektion von sog. Lupus-Antikörpern. Lupus-Antikörper werden derzeit durch eine lupussensitive PTT detektiert, jedoch gibt es immer wieder grenzwertige oder schwer interpretierbare Analyseergebnisse. Um hier eine verbesserte Diagnostik anzubieten, wird nun auch die KCT analysiert. Liegt das Ergebnis unter 100 Sekunden, so kann man einen Lupus-AK ausschließen. Ist der Wert größer als 100 Sekunden wird der sog. Rosner-Index angeschlossen. Dieser errechnet sich wie folgt:
Rosner Index = [KCT (50:50 - Mischung aus PP und NP) – KCT (NP)] / KCT (PP)
NP: Normal-Plasma
PP: Patienten-Plasma
Ergibt sich hier ein Wert unter 0.15, ist das Vorliegen eines Lupus-AK ebenfalls eher unwahrscheinlich. Ist der Wert jedoch größer 0.15, bestätigt dies einen Lupus-AK.
CAVE: Die Diagnose eines Antiphospholipid-Syndroms darf nur gestellt werden, wenn
1. ein begründeter klinischer Verdacht besteht
UND
2. Anti-Cardiolipin-AK, ß2-Glykoprotein-AK, oder Lupus-AK nachweisbar sind
UND
3. die entsprechenden AK nach 12 Wochen weiterhin bestehen.
Referenzen:
Miyakis S, Lockshin MD, Atsumi T, et al. International consensus statement on an update of the classification criteria for definite antiphospholipid syndrome (APS). J Thromb Haemost 2006; 4: 295–306.
Benötigtes Material: Citrat-Plasma
Anforderungsschein: G-Schein
Analysehäufigkeit: Mo-Fr zu den Routinelaborzeiten
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Orgaran-Monitoring
(13.5.2008)
Ab sofort ist es möglich in unserem Labor den Orgaran-Wirkspiegel indirekt mittels eines adapdierten Anti-Xa Tests bestimmen zu lassen.
Orgaran (Danaparoid-Natrium) wird v.a. bei Patienten mit HIT Typ II als antikoagulative Alternative zu den Heparinen (UFH / NMH) eingesetzt. Zu beachten ist allerdings, das in vitro circa zehn Prozent der HIT-Typ-II-Patienten eine Kreuzreaktion mit Danaparoid-Natrium zeigen.
Je nach Indikation sind Dosieruing, sowie anzustrebender Anti-Xa Bereich (in IU/ml) unterschiedlich.
Mehr zu diesem Thema lesen sie bitte in der Rubrik Nützliches/Dowloads > Gerinnung
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Umstellung auf einen neuen D-Dimer Test
(27.11.2007)
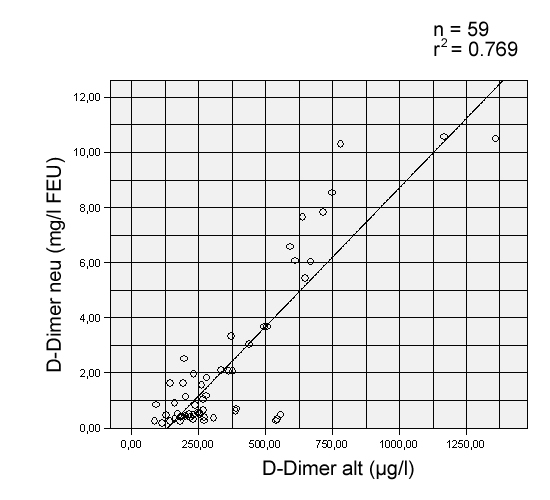
Unser Labor hat am 12.12.2007 auf den neuen Innovance D-DIMER-Assay von Dade Behring umgestellt.
Mit dieser Umstellung ist die Einführung eines neuen Cutoffs verknüpft:
Der neue D-DIMER Test hat folgende Leistungsdaten:
Ein weiterer Vorteil ist, dass durch ein Zusatzreagenz Störungen durch sogenannte heterophile Antikörper eliminiert werden.
Dies bedeutet z.B. keine fälschlich erhöhten D-Dimer Spiegel durch Rheumafaktoren oder Anti-Maus-Antikörper.
Im Vorfeld haben wir eine Korrelation des alten und des neuen D-Dimers durchgeführt (s. Bild)
Für weitere Fragen steht Ihnen Herr Dr. Cadamuro unter der Klappe 57263 (alternativ 3807) gerne zur Verfügung.
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Multimerenanalyse des von Willebrandfaktors
(31.7.2007 - Update: 5.1.2010)
Die Multimerenanalyse des von Willebrand Faktors dient zur Diagnostik und Differenzierung der unterschiedlichen Subtypen des von Willebrand Syndroms. Bei klinischem Verdacht UND entsprechenden Laborwerten (von Willebrand Antigen, Ristocetin-CoFaktor, Kollagen Bindungsaktivität, ... erniedrigt) ist eine solche Analyse angezeigt.
Da dies eine sehr aufwendige Analyse ist, die außerdem einer großen Erfahrung bedarf, soltte sie nur speziellen Zentren vorbehalten bleiben.
Die Multimerenanalyse ist am G-Schein online anforderbar. Bitte geben sie auch eine kurze Anamnese mit an, da diese die Befundung der Ergebnisse erheblich erleichtert.
Das Resultat wird dem Zentrallabor zur Archivierung geschickt und sofort an sie weitergeleitet.
Ungefähre Dauer bis zur Befundübermittlung: 4 Wochen.
Für den Inhalt verantwortlich: Dr. Janne Cadmuro
Heparin induzierte Thrombozytopenie Typ 2 (HIT II)
(20.6.2005)
Bei der HIT II kommt es 5-10 Tage nach Heparingabe zum Thrombozytenabfall, welcher aber fast nie Werte unter 20G/L erreicht. Bei vorangegangener Heparingabe in den letzten 30-90 Tagen kann eine Sensibilisierung stattgefunden haben und ein Thrombozytenabfall daher bei wiederholter Gabe schneller erfolgen.
Ursächlich für diese Erkrankung sind Antikörper gegen den Heparin/Thrombozyten-Komplex. Diese Antikörper können in unserem Labor nachgewiesen werden und sind für diese Erkrankung beweisend.
Therapeutisch wird schon bei einem Verdacht auf eine HIT II eine Umstellung der Antikogulation auf Heparinoide o.Ä. empfohlen.
Falls Sie uns eine Probe zur Abklärung schicken wollen, würden wir sie bitten dies telefonisch anzumelden und vor 12:00 in Labor zu bringen, da dies eine sehr aufwendige und Zeit konsumierende Erkrankung ist.
Weiters würden wir sie bitten unsere Scorecard auszufüllen und mitzuschicken. (Download)
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Erweiterte Verfügbarkeit der Faktor VIII und Faktor IX Analysen
(20.6.2005)
Ab sofort können Faktor VIII und IX täglich (also auch am Wochenende) von 8:00 bis 20:00 h durchgeführt werden. Messungen außerhalb des Routinebetriebes, also wochentags von 16:00 bis 20:00 h und an Wochenenden, können nur bis zu Werten von 10% und nicht darunter erfolgen. Daher ersuchen wir, dass Proben von bekannten Hämophilie-Patienten zu den Routinezeiten (Wochentags 8:00-16:00) gesendet werden, damit auch Messungen mit Werten <10% durchgeführt werden können.
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Faktor VIII-Inhibitor
(20.6.2005)
Die Bestimmung des Faktor VIII-Inhibitors nach der Bethesda-Methode wird nun auch im Zentrallabor durchgeführt und muss nicht mehr verschickt werden.
Ein Faktor VIII-Inhibitor ist ein Antikörper gegen den Gerinnungsfaktor VIII mit der Folge eines Mangels desselben und den daraus resultierenden Gerinnungsstörungen („Hemmkörper-Hämophilie“). Ursächlich für einen solchen Inhibitor sind meistens exogen zugeführte Faktor VIII-Präparate bei Hämophilie A-Patienten. Mittels der Bethesda-Methode können Hemmkörper quantifiziert werden, wobei eine Bethesda-Einheit (Bethesda-Unit/BU) diejenige Inhibitoraktivität ist, welche 50% des vorhandenen Faktors inaktiviert.
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Antiphospholipid-Screening
(20.6.2005 - Aktualisierung 9.4.2009)
Autoantikörper gegen spezifische Phospholipide beeinflussen die Gerinnung im Sinne einer Verlängerung der PTT und paradoxerweise einer Thromboseneigung (Die Ursache hierfür ist noch nicht geklärt). Auch die Inzidenz von Aborten ist bei positiven Anti-Phospholipid-Antikörpern erhöht. Die Diagnose „Anti-Phospholipid-Syndrom“ und deren Klassifizierung erfolgen nach einem 1998 getroffenen Konsensus. Pathogenetisch ist die Bildung dieser Antikörper unklar. Der Verlauf hinsichtlich Antikörpertiter ist sehr variabel und reicht von Spontanremissionen bis zu dramatischen Anstiegen innerhalb kurzer Zeit.
Zu den wichtigsten Antikörpern aus dieser heterogenen Gruppe gehören:
Weitere Phospholipide, die in einem weiteren Test miterfasst werden können, sind:
Bei diesen Untersuchungen werden jeweils IgG- und IgM-Antikörper bestimmt, sodass auch eine zeitliche Aussage getroffen werden kann.
Indikationen zum APS-Screnning:
ergänzend zur Lupus-Antikörper-Diagnostik bei:
Bei der Anforderung eines "Antiphospholipid-Screenings" (s. G-Schein) werden standardmässig folgende Analysen durchgeführt:
Da Anti-Phospholipid-Antikörper auch passagär bei Infekten (häufig bei Kindern) auftreten können, sollen zur sicheren Diagnosestellung die Antikörper in 2 Blutproben, die in einem zeitlichen Abstand von mindestens 12 Wochen abgenommen wurden, nachgewiesen werden.
Literatur:
Wendell et al. International consensus statement on preliminary classification criteria for definite antiphospholipid syndrome. Arthritis & Rheumatism 1999; 42:1309-1311
Lackner et al. Revision of the Sapporo criteria for the antiphospholipid syndrome – Coming to grips with evidence and Thomas Bayes?, Thromb Haemost 2006; 95: 917–9
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Aspirin- / Plavix-Monitoring
(20.6.2005)
ASS ist ein wirksamer irreversibler Hemmer der Thrombozytenaggregation und wird daher oft als Prophylaktikum nach thrombembolischen Geschehen verabreicht. Jedoch sind rund 20-30% aller Europäer „ASS Non-Responder“. Bei diesen Patienten hat ASS keine oder eine verringerte Wirkung auf die Throbozytenaggregation. Um Non-Responder frühzeitig zu erkennen und dadurch die Gefahr für ein mögliches Rezidivgeschehen zu verringern, kann die Thrombozytenaggregation bei Patienten mit ASS-Behandlung untersucht werden. Diese Messung ist auch geeignet, andere Arten der medikamentösen Hemmung der Thrombozyten-Aggregation (Plavix, Tiklid, Reopro, etc) sowie pathologische Veränderungen der Thrombozytenfunktion (von Willebrand Syndrom, Bernard Soulier Syndrom, Storage pool disease, Mb. Glanzmann, etc) nachzuweisen.
Da die Bestimmung der Thrombozytenaggregation sehr empfindlich ist, ist die Präanalytik von großer Wichtigkeit. Präanalytische Störfaktoren sind eine forcierte Abnahme, zu langes Stehenlassen der Probe (die Probe muss innerhalb von max. 2 Stunden gemessen werden), mechanische Belastung (keine Rohrpost !) und Kälte.
Für etwaige Rückfragen bzgl. neuer oder bestehender Gerinnungsanalysen rufen Sie bitte
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Benachrichtigung über die Übernahme der speziellen Gerinnungsanalysen, sowie der Antikoagulantieneinstellung durch das Zentrallabor
(7.3.2005)
Hiermit dürfen wir Ihnen mitteilen, dass die gesamte Gerinnungsanalyse, also auch spezielle Gerinnungsparameter ab 7.März 2005 im Zentrallabor durchgeführt wird.
Präanalytik:
Weiters möchten wir Ihnen mitteilen, dass nun auch die Einstellung der mit Cumarinderivaten antikoagulierten Patienten künftig im Zentrallabor (Gerinnungslabor - Erdgeschoß) erfolgen wird.
Die Ambulanzzeiten hierfür bleiben vorläufig unverändert: Mo-Do. 7.30-9.00
Für etwaige Rückfragen rufen Sie bitte:
Gerinnungslabor (3807)
Dr. J. Cadamuro (57263)
Dr. B. Lackner (57261)
Für den Inhalt verantwortlich: Dr. Janne Cadamuro
Heparinmonitorisierung
(20.7.2002)
Da Heparin die Inaktivierung von Gerinnungsfaktor Xa und Thrombin durch Antithrombin III beschleunigt, finden unfraktionierte und niedermolekulare Heparin-Präparate verbreitete therapeutische Anwendung als Antikoagulantien. Aufgrund verschiedener Einflüsse kann die pharmakologische Heparinwirkung von Patient zu Patient trotz gleicher Dosierung schwanken. Mit diesem Test kann die Therapie sowohl mit niedermolekularen (LMW) als auch mit unfraktionierten Heparin-Präparaten verfolgt werden. Der therapeutische Bereich bewegt sich zwischen 0,4 – 0,8 IU/ml. Der prophylaktische Bereich ist indikationsabhängig, wird jedoch häufig mit 0,2 - 0,4 IU/ml angegeben. Bei Werten, die um 1,0 IU/ml und darüber liegen, erhöht sich die Gefahr für Blutungskomplikation.
Das Probenmaterial ist Citratplasma (1 Teil 0,11 mol Natriumzitrat + 9 Teile Blut). Die Bestimmung wird mittels A-Schein angefordert und ist auch im Notfall erhältlich.
D-Dimer, quantitativ, im Zitratblut:
D-Dimer ist das primäre Abbauprodukt von vernetztem Fibrin. Eine erhöhte Konzentration von D-Dimer im Plasma kann auf ein akutes thrombotisches Geschehen hinweisen. Die klinische Utilität von D-Dimer liegt unter anderem im Ausschluß einer tiefen Beinvenen-thrombose und einer pulmonalen Embolie. Es besteht eine umfangreiche Literatur über Sensitivität und Spezifität von D-Dimer-Erhöhungen im Plasma bei verschiedenen Krank-heitsbildern. Der Großteil der Studien weist auf eine Sensitivität und einen negativen Prä-diktivwert für die tiefe Beinvenenthrombose und die pulmonale Embolie im Bereich von 90-100 % hin, während die Spezifität und der positive Prädiktivwert im allgemeinen unter 50% liegen und von verschiedenen Merkmalen der Population, z.B. dem Alter, abhängig sind.
Die Methode beruht auf einer turbidimetrischen Messung der Antigen-Antikörperreaktion nach dem Endpunktprinzip. Das Probenmaterial ist Zitratplasma (1 Teil 0,11 mol Natrium-zitrat + 9 Teile Blut). Bei der venösen Blutabnahme muss darauf geachtet werden, dass der Staudruck den systolischen Druck nicht übersteigt und höchstens 1 Minute dauert. Der Stauvorgang an der gleichen Vene soll innerhalb von 10 Minuten nicht wiederholt werden. Der Referenzbereich liegt unter 0,5 µg Fibrinogen Äquivalenten pro ml Plasma. Die Be-stimmung wird auf dem A-Schein angefordert und ist auch für den Notfall verfügbar (Not-fallschein).
G-A Polymorphismus, Prothrombin-Gen
Zahlreiche kürzlich veröffentlichte Studien haben gezeigt, dass eine G-A Transition in Posi-tion 20.210 in der 3’ nicht translatierten Region des Prothrombin-Gens mit einer erhöhten Prävalenz von Venenthrombosen und auch mit einem erhöhten Prothrombinspiegel im Plasma assoziiert ist. Während in gesunden Kontrollen die Frequenz des variablen A-Allels bei 1% oder darunter liegt, lag die Frequenz dieses Allels in Patienten mit venösen Thrombosen zwischen 3 und 9% in verschiedenen Studienpopulationen. Einzelne Berich-te weisen auch auf Zusammenhänge dieses Polymorphismus mit Myocardinfarkt in jun-gen Patienten hin, während andere Studien eine diesbezügliche Assoziation nicht beo-bachteten.
Zur Durchführung der Bestimmung sind 2 ml EDTA-Blut notwendig. Da es sich um eine gentechnische Untersuchung handelt, sind die Vorschriften bezüglich Patientenberatung und Datenschutz gemäß GTG(Gentechnikgesetz) § 61 - 71 einzuhalten. Die Anforderung erfolgt am B-Scheines.



